Возможности генетического тестирования в практике врача-трихолога
 |
|
Сафонова Лариса Алексеевна
|
Записано по материалам доклада Сафоновой Л.А., представленном на сателлитном симпозиуме «Трихология для косметологов» в рамках выставки профессиональной косметики и оборудования для салонов красоты INTERCHARM professional 2015.
Лариса Алексеевна Сафонова в своем докладе затронула одну из актуальных проблем современной медицины. По ее словам, в настоящее время большое внимание уделяется медицине будущего, или 4П-медицине.
4П-медицина — термин, предложенный американским профессором Лероем Худом, основателем Института системной биологии и 4П-медицины. Концепция «четырех П» состоит из следующих характеристик медицины:
Предиктивная (to predict (с англ.) - предсказывать) — способная предсказывать развитие болезни еще до клинических проявлений.
Персонализированная (to personalize (с англ.) - персонализировать) — данный аспект в большей части относится к фармакотерапии и назначении медикаментозного лечения с учетом генотипа.
Превентивная (to prevent (с англ.) - предупреждать) — направленная на предупреждение заболевания.
Партисипативная (to perticipate (с англ.) - участвовать) — пациент является активным участником собственного лечения, его информируют и обучают, помогают в выборе.
4П-медицина базируется на достижениях биомедицинской науки последних лет, в особенности на генетике. Предполагается, что генетика станет основой профилактики и лечения заболеваний.
Некоторые заболевания волос имеют генетическую основу и экогенетическую сверхсоставляющую. Для того, чтобы определить генетическую основу заболевания имеются различные методы генетических исследований. И наиболее полномасштабный метод исследования полногеномный поиск ассоциаций.
Полногеномный поиск ассоциаций
Полногеномный поиск ассоциаций (GWAS – genome – wide – association study) – исследование ассоциаций между геномными вариантами и различными фенотипическими проявлениями. Анализ ассоциаций генов-кандидатов лежит в основе идентификации генетических вариантов предрасположенности.
Известно около 90 наследуемых заболеваний и синдромов, сопровождающихся алопецией или гипотрихозом. В большинстве случаев врожденный гипотрихоз является одним из признаков эктодермальных дисплазий, изолированных или сочетанных. В тех случаях, когда изменения волос доминируют и имеют большое диагностическое значение, их рассматривают как отдельное заболевание.
Затем Сафонова Л.А. подробнее рассмотрела некоторые заболевания волосистой части головы.
Монилетрикс
 |  |
Это заболевание генетически гетерогенно. В большинстве случаев наследуется по аутосомно-доминантному типу. У мальчиков заболевание встречается чаще, чем у девочек.
Клинические признаки заболевания:
-
гипотрихоз, повышенная ломкость и поредение волос
-
нарушение ороговения волосяных фолликулов с образованием фолликулярных гиперкератотических узелков.
На трихоскопии: чередование перетяжек веретенообразных вздутий на стержнях волос.
Лечение заболевания:
-
как правило, любое лечение малоэффективно
-
назначают поливитаминные препараты
-
физиотерапевтические процедуры
-
кратковременно, до уменьшения выраженности фолликулярного кератоза, назначают витамин А в дозах около 100 000 ЕД или неотигазон в дозе 0,5 мг/кг.
Синдром Нетертона
 |  |
Наследуется аутосомно-рецессивно. Обнаружены мутации в гене SPINKS 5q32 первичным продуктом которого является фермент-ингибитор серин-протеазы Kazal type 5, который в норме определяется в эпителиальной и лимфоидной тканях.
Предполагается нарушение формирования липидного барьера кожи, а именно его ламеллярной субстанции, что проявляется снижением резистентности к бактериальным патогенам и повышенной склонностью к воспалительным процессам.
Клинические признаки заболевания:
-
гипотрихоз. повышенная ломкость волос
-
ихтиозиформные изменения кожи
-
атопический дерматит
На трихоскопии: характерные изменения стержней волос - «бамбуковые волосы»
Лечение заболевания:
-
симптоматическое. Новорожденные не редко нуждаются в интенсивной терапии, лечении системными антибиотиками.
-
наружно назначают слабые кератолитические средства, мази и кремы с кортикостероидами, ретиноидами.
-
системные ретиноиды следует применять с осторожностью ,у ряда больных на их фоне возможно обострение процесса.
Врожденный наследственный гипотрихоз
Заболевание наследуется по аутосомно-доминантному типу. Происходит миниатюризация волос и замена терминальных волос пушковыми. Встречается редко.
Клиническое проявление заболевания:
-
волосы с рождения редкие, легко обламываются.
-
в раннем детстве становятся более густыми, но примерно с пубертатного возраста практически полностью выпадают сначала в теменной области, а затем и по краям.
-
характерна высокая лобная и затылочная линия волос. Может развиваться тотальная алопеция особенно у мужчин
-
зубы и ногти не изменены
-
в зоне поражения могут быть признаки перифолликулярного рубцевания
-
с рождения выявляются милиарные кисты
-
примерно у 50% больных выявляется увеличенная щель между центральными резцами верхней челюсти (диастема).
-
возможно сочетание заболевания с атопическим дерматитом, синдромом Черногубова-Элерса-Данлоса, наследственной ювенильной дистрофией сетчатки.
Трихотиодистрофия
 |
Трихотиодистрофия представляет собой заболевание из группы нейроэктодерманых дисплазий. Развитие болезни объясняют дефицитом серы.
Однако, уровень серосодержащих аминокислот в крови в пределах нормы, что исключает алиментарный этиологический фактор.
Наследуется по аутосомно-рецессивному типу.
Клинические проявления заболевания:
-
гипотрихоз, повышенная сухость и ломкость волос
-
структурные нарушение стержней волос
-
снижение содержания серосодержащих аминокислот в стержнях волос на 10-50%
-
ихтиозиформные изменения кожи
-
задержка умственного и физического развития, преждевременное старение
-
врожденная двусторонняя катаракта
-
неврологические нарушения
-
повышенная фоточувствительность
Диагноз ставят на основании клинической картины, данных микроскопии волос, анализа микроэлементарного состава волос.
Синдром Менкеса
 |  |
Развитие синдрома связано с дефицитом меди вследствие нарушения ее абсорбции. Заболевание наследуется рецессивно, сцеплено с Х-хромосомой. Нарушается работа АТР фермента, обеспечивающего доставки CU2+. Значительное снижение содержание меди отмечается в сыворотке крови, ткани мозга и печени. В плазме резко снижено содержание церулоплазмина. В то же время высокие концентрации Сu2+ обнаруживают в тканях пищевода, почек, легких, селезенки, поджелудочной железы, коже и мышцах. В основном болеют мальчики.
Клинические проявления заболевания:
структурные аномалии стержня волос, гипотрихоз
тяжелая умственная и физическая отсталость
задержка роста и патология костной ткани
судороги
высокая подверженность инфекциям
аномалии почек и сосудов, зрительные расстройства
диагноз ставят на основании клинической картины, данных световой микроскопии волос, биохимического анализа крови
Важно своевременное распознавание болезни, так как парентеральное введения препарата Cu2+ дает обнадеживающие результаты только при очень раннем их назначении — в течение первого месяца жизни.
При уже возникших изменениях в ЦНС клинического эффекта не наблюдается, даже при нормализации уровня Cu2+ в плазме крови.
Синдром неукладываемых волос
Синдром неукладываемых волос имеет аутосомно-доминантный тип наследования. В основе изменений формы волосяного стержня лежит нарушение кератинизации и изменение конфигурации внутреннего корневого влагалища.
Клинические проявления заболевания:
-
волосы светлые, с серебристым оттенком
-
они довольно густые, скорость их роста не замедлена, повышенной ломкости нет
-
после расчесывания волосам не удается придать желаемую форму
-
иногда наблюдается слабо выраженные дефекты зубной эмали и ногтевых пластин
-
при более тяжелом течении синдром может сочетаться с пигментной дистрофией сетчатки, катарактой, олигодонтией, брахидактилией
Диагноз устанавливается на основании клинической и гистологической картины, а также характерных ультраструктурных признаков (на поверхности волоса определяется продольное углубление, а поперечный срез имеет вид почки или треугольника, иногда - уплощенного элипса.
Гнездная алопеция (ГА)
 |  |
ГА — хронический мультифактериальный дерматоз, обусловленный аутоиммунным поражением клеток волосяного фолликула, развивающийся на фоне генетической предрасположенности и характеризующийся образованием очагов выпадения волос и частым поражением ногтевых пластин.
Гены, связанные с ГА
Angela Christiano et al. (2010) обнаружили корреляцию между геном ULBP3 на 6 хромосоме в локусе q25.I и ГА. В норме этот ген не выделяется, но при ГА ULBP3 белки обнаруживаются в большой концентрации в ВФ. ULBP3 соединяется с рецепторами NK — клеток, называемых NKG2D, вызывая перифолликулярное воспаление. ULBP3 гены могут быть использованы в качестве биомаркеров при ГА.
Выделяют и другие гены, которые некоторые ученые связывают проявлениями ГА.
Так исследователи указывают на ген EDA2R, мутации в котором приводят к потере волос.
Выявлены гены, которые участвуют в потере волос и влияют на структуру волос. Одним из этих генов является ген P2RY5. При мутации в данном гене в волосяном фолликуле происходят определенные биохимические процессы, приводящие к сухости, ломкости и поредению волос.
В 2009 году в Японии был обнаружен ген SOX21 , который помогает регулировать процесс синтеза кератина и, таким образом, является ведущим регулятором формирования волос.
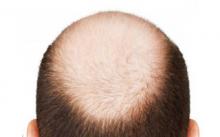
Андрогенетическая алопеция (АГА)
 |  |
АГА — поредение волос, возникающее в результате генетически обусловленной повышенной чувствительности волосяных фолликулов к мужским гормонам. Выявлена ассоциация АГА и с ишемической болезнью сердца, артериальной гипертензией, ожирением, раком простаты и др.
Механизм развития АГА и гены
Тип наследования - полигенный. Андрогенный ген AR, влияющий на мужское облысение, наследуется по линии хромосомы Х, передаваемой по материнской линии и находится в положении Хq12. Второй ген расположен на 20й хромосоме 20р11.22. Третий — 3q26, расположен на 3й хромосоме. Второй и третий гены могут быть унаследованы как от отца, так и от матери.
Ген AR расположенный на Х-хромосоме в положении Хq12 является рецептором андрогенов. Его функцией является метаболизм стероидных гормонов. Андрогеновый рецептор является внутриклеточным фактором транскрипции, который активизируется путем связывания с тестостероном. При связывании с гормоном, рецептор перемещается в ядро и связывается со специфичной последовательностью молекулы ДНК. Связанный комплекс тестостерон — AR активирует или подавляет экспрессию тестостерон-регулирующих белков. Основные — полиморфизмы — CAG повторы в 1 экзоне.
Значение исследования CAG повторов гена AR в общей практике
Исследования полиморфизма CAG-повторов в 1 экзоне гена андрогенетического рецептора (AR) имеет диагностическое и прогностическое значение, позволяющее определить риск репродуктивных нарушений, рака простаты, установить причину мужского бесплодия, мышечной атрофии.
-
Диапазон 20 — 26 повторов считается относительной нормой. При уменьшенном количестве CAG-повторов (<18) в гене AR отмечается повышенная чувствительность к андрогенам и увеличивается риск рака простаты. А у женщин в этом случае отмечается повышенный риск развития рака молочной железы, причем более агрессивной формы, рака эндометрия, СПКЯ и гиперандрогении.
-
Увеличение количества CAG-повторов (>26) свидетельствует о наличии генетической предрасположенности к гормонозависимому нарушению сперматогенеза.
-
Увеличение числа CAG-повторов до 38 — 62 приводит к спинобульбарной мышечной атрофии типа Кеннеди.
Результаты генетического теста позволяют врача внедрять предсимптоматическую оценку риска, что позволяет провести раннюю диагностику и предотвратить наступление заболевания, предложив персонализированные рекомендации. Синтез традиционных методов обследования и результатов генетического тестирования позволяет персонифицировать рекомендации по применению лечебных мероприятий и их длительность.
Метки
монилетрикс синдром Нетертона врожденный наследственный гипотрихоз трихотиодистрофия синдром Менкеса синдром неукладываемых волос гнездная алопеция андрогенетическая алопеция АГАКомментарии
- Вконтакте